泰博医疗-专业的儿科医疗连锁机构
作者: 发布时间:2016-10-13 转至微博:
|
医药网9月28日讯 在《关于开展仿制药质量和疗效一致性评价的工作意见》(国办发[2016]8号)下发之后,国务院、CFDA、中检院先后发布了20余个相关公告,公告涉及一致性评价的各个环节,从发布公告的频度和密集程度可以看出此项一致性评价工作不同于以往工作的特点,相当严肃且相当紧迫。并且,开展仿制药一致性评价工作业已被列入“十三五”规划重点任务,上升到了国家战略层面。面对这项工作,仿制药企“家家有本难念的经”,选择哪些品种开展一致性评价是其中一个关键的难点问题。
背景与难度
1、必然性
淘汰行业低端产能,仿制药一致性评价是推进供给侧结构性改革的重大举措。目前国内原研药在大医院销售占比高达80%,仿制药质量参差不齐,提高仿制药质量,临床上实现与原研药相互替代,才能够推动药品生产领域的结构性变革。据了解,国内仿制药行业毛利率不到10%(国际平均水平约为40%-50%),而且过半品种高度重复。
一致性评价是提升国产仿制药国际竞争力的必由之路,也是缓解国内医保、药价新政压力的必然选择。
仿制药与原研药一致性是国际通行原则,一致性评价是很多国家都走过的路。上世纪70年代,美国启动仿制药生物等效性评价,开始关注仿制药的疗效,历时10年,淘汰6000种未通过一致性评价的药品。英国曾对3.6万种药品进行一致性评价。日本则于上世纪90年代末启动药品品质再评价工程。上述三个国家都实现了仿制药产业的升级,药品质量、行业生态、工业价值得以显著提升。我国2001年修订的《药品管理法》,把仿制药集中到国家统一审批,开始要求仿制药作临床试验;2007年鼓励仿制原研药,但还不是强制性要求。《国家药品安全“十二五”规划》印发时,提出了仿制药与原研药质量一致性评价的任务;去年国务院的44号文,提出质量疗效与原研药一致的要求。一致性评价,在国内可以说是“补课”。
2、选择难度
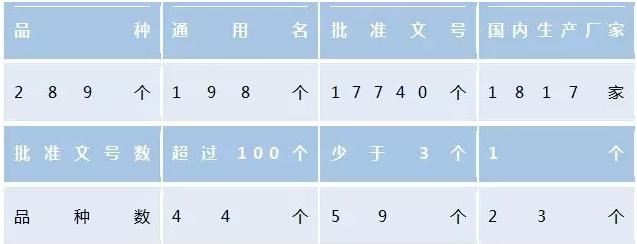
笔者梳理发现,目前首批需要在2018年底完成一致性评价的基本药物口服制剂品种289个,通用名198个,涉及批准文号17740个,国内生产企业1817家,进口企业42家(见表1)。批准文号的品种重复性极高,一个品种超过300个品准文号的有16种,100个批准文号的有44种。仅复方磺胺甲噁唑片,共有895个文号、869家企业生产。如果企业对所有的批准文号都进行一致性评价,显然不现实,评价时间也有限,每一品种的评价费用约为500万-600万元。基药2015年整个销售收入按全部药品销售收入的40%来计的话,一致性评价所花的费用大约会超过基药全年整个销售收入的20%。那么,企业面临的问题也就出来了:到底要不要做?做哪些?先做哪些?如何选择?
经济学是专门研究选择的学科,经济学对资源配置选择依据是商品的价值,需要分析药品的价值到底包括哪些、如何根据药品的价值做出合理的选择。
表1:首批需要在2018年底完成一致性评价的基药口服制剂品种基本情况
 药品的价值内涵与构成
首先看商品价值。宏观意义上讲,商品价值包括两部分:一部分是商品内在的使用价值,反映商品的本质属性——用途是什么;另一部分是商品的市场价值,反映其社会属性,人们愿意为获得使用价值而付出的代价。商品的使用价值需要通过市场价值来体现,同时市场价值更多反映的是消费的意愿和需求。
药品价值同样包括使用价值和市场价值,使用价值就是药品本身的功能,用于治疗、诊断、预防人的疾病,也就是药品的使用价值来自于临床;市场价值则是这种临床价值的消费意愿和需求,也就是人们对健康改善或健康水平提高愿意付出的代价。药品关乎人的健康与生命安全,因此其还具有更多的公益性和社会福利属性,药品行业的发展直接关乎政府的公信力,由此,药品还具有另外一个特殊的价值,就是社会价值。
1、临床价值
这是药品最核心的价值,是决定市场价值和社会价值的基础。国际上,很多国家(如德、法等)非常关注药物的临床价值,将其作为药品相关决策的重要依据,如药品的定价、医保目录的遴选、临床用药指南的制定等。
德国从2011 年实施的《行业改革法案》( AMONG),将创新药品的附加效益划分为重大、显著、较小、附加效益不可量化、不具有附加效益和效益低于对照疗法6个等级,前3个等级药品具有附加效益,后3个等级不具有附加效益,同时规定如果药品附加效益不被接受,则将该药划入参考价格组来确定医保支付价格,如果具有附加效益则药企可以和基金委员会协商确定医保支付价格,往往要比参考价格组确定的价格高出很多。附加效益的判断标准依据就是临床价值,其判定指标是全因死亡率、发病率、健康相关生命质量和不良反应这4个指标。新药制定价格时要求递交卷宗,由早期效益评估研究院依据这4项临床价值指标对卷宗进行评估,评价其相对于对照疗法的附加价值程度。
在法国,新药进入市场需要经过3道程序——上市审批、价值评估和价格协商。如果药品获得上市许可,将由卫生最高委员会和透明委员会进行治疗价值评估,并对治疗价值提高程度进行评级(ASMR分级)。在透明委员会评估的基础上,健康产品经济委员会与药企协商价格(包括零售药价格和用药价格)。ASMR分级过程也是对药品临床价值判断的过程,依据主要指标是包括:药物的安全性、有效性、质量可控性、依从性、创新性、满足社会需求和其他社会特性。ASMR分级直接决定药品出厂价格高低,创新药品为ASMRI至ASMRⅢ级,常规药品为ASMRIV或ASMRV级,每一级别的价格差约为30%。纳入医保目录的药品需达到ASMRⅣ以上,ASMRV的药品要想纳入目录,需要比同类药品廉价才可以。
关键词:
|