泰博医疗-专业的儿科医疗连锁机构
作者: 发布时间:2015-10-26 转至微博:
|
医药网10月26日讯 分析2000年至2014年FDA优先审评品种,优先审评究竟有何益处?截至2015年9月中旬,我国有数以千计的申请获得特殊审批资格,但特殊审批之于畅销药,又有多大的相关性?
美国是全球创新能力最强的国家,很多人都将这一现象归结于其制度、人才培养、知识产权保护以及强大的经济基础支撑等方面的优越性,还有美国国内庞大而灵活的私人及企业科技研发机构,带动了整个国家科技的蓬勃发展。在药物创新研发方面,美国也长期引导全球潮流,原因一是美国人骨子里非常崇尚的创新精神,二是政策方面也为发明和创造者提供了适宜的环境。
为了研制出能够战胜疾病的新药,不计其数的科学工作者耗费数年到数十年的时间在各自岗位辛勤工作,由此源源不断的新药注册申请送到了FDA手中。为加快审查,从1992年开始,FDA创建了审查时间两级系统(标准审评和优先审评)——优先审评(Priority Review)的周期为6个月,标准审评周期为10个月。通过增加人力物力的投入,优先审评类药物审评的速度得以提高。
要想获得优先审评资质的认定,申报的产品必须在安全性和有效性上产生显著改善或具有优于现有治疗手段的潜力,更方便或适用于更广泛的人群。与加速审批等不同,优先审评的特点只针对审评阶段,它既不改变审评标准,也不加速临床试验进程。但是,新药进入市场的时间缩短了,利于企业更快收回投资。
曾有研究数据显示,创新性程度越高的药品,取得的经济回报也越大。回望2000年至2014年FDA优先审评品种,哪些产品获得了巨大经济回报?而对于那些熟悉的畅销药物,优先审评有何益处值得考究。
美国:优先审评药未必畅销
畅销药的成因主要是药物特性、市场规律、企业营销实力及专利等,优先审评资格非主因
2000~2014年,共有301个品种获得FDA的优先审评资质,其中2014年获批最多,为37个,而排第二位的年份要追溯到2004年的29个;获批最少的是2001年,只有10个。
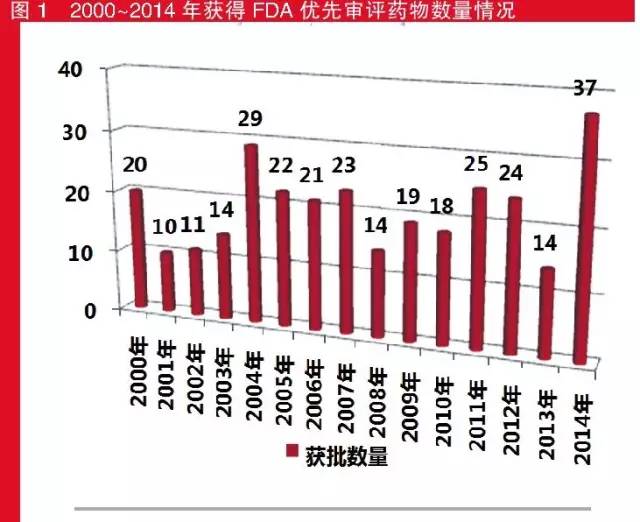 值得注意的是,在2006年至2008年间,由于艾滋病的泛滥,FDA临时性优先审评批准了20个治疗此类疾病的药物。
在获得优先审评资质的药物中,新分子实体(NME)占据了半壁江山。
既获得优先审评又获得孤儿药称号的“双获”药物则是另一个值得关注的现象。从数量上看,优先审评药物中新分子实体和获得孤儿药称号数量最多的年份均为2014年,分别为19个和18个;而从占比来看,新分子实体数量占比最高的是2001年,孤儿药占比最高的是2014年。15年间,有7个年份的NME获批数量的占比超过了五成,获孤儿药称号的药物的占比在2014年也接近50%,且近几年(2013年除外)这种“双获”药物的数量均超过了两位数。
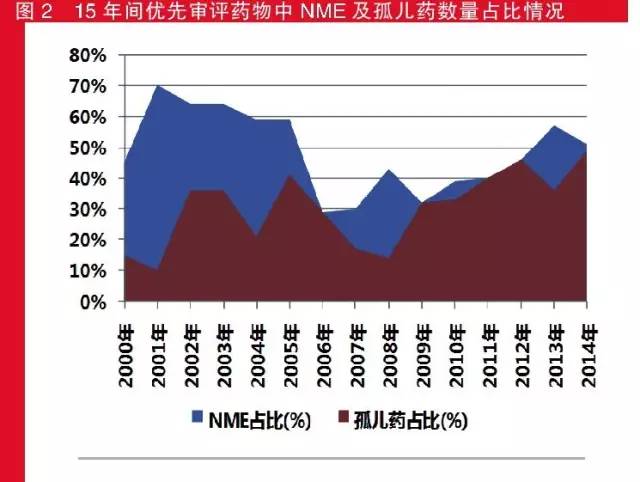 追踪近些年来受市场追捧的超级畅销药可以发现,虽然有近三成的药物获得了优先审评资格,但超级畅销药最显著的特点却不是优先审批资格,而是它们的身份大多是新分子实体和新生物药,且大多属于制药巨头。
关键词:
|