泰博医疗-专业的儿科医疗连锁机构
作者: 发布时间:2015-06-05 转至微博:
|
医药网6月4日讯
1.在审评
本周(2015.5.24-2015.5.30)新进申报45个药物(按受理号计,不含复审和补充申请,下同),其中1个中药,1个生物制品。以下具体介绍重点化药:
1.艾普拉唑:本品是丽珠制药从韩国一洋手中获得的,为1.1类新药,最早2008年上市,也是丽珠的主打产品之一。艾普拉唑是一种PPI类药物,用于治疗胃、十二指肠溃疡等相关疾病。在国内一直由其独家销售,且目前只有片剂上市,丽珠制药的注射剂也处于临床中,现在PPI类药物大户江苏奥赛康终于出手,申报艾普拉唑钠及其注射剂,也想分一杯羹啊。
2.非诺贝酸胆碱缓释片:本品是一种降血脂的药物,非诺贝特的替换产品,国内均已3.1类申报,沈阳华泰此次1.6类申报新的国内外均无的适应症,推测是降血脂相关的,具体还要等做临床或者上市才知晓。
3.尼洛替尼:本品是慢性髓性白血病的二线用药,诺华早在2009年就已在国内进口上市,只是不知为何一直没有企业申报,江苏豪森本周3.1类提交盐酸尼洛替尼的原料药,系国内首家仿制申报。
2.在审批
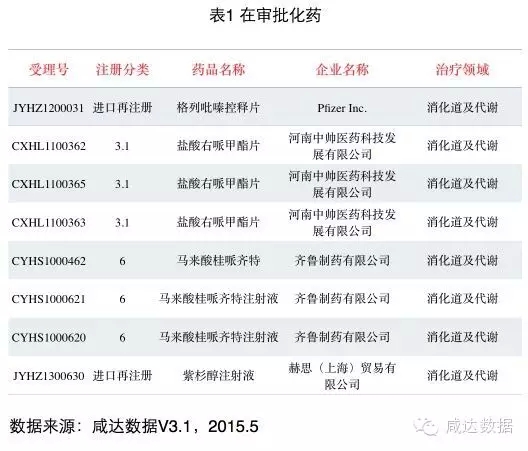
本周共8个药物进入审批程序,均为化药:
1.盐酸右哌甲酯:本品用于治疗注意力缺陷多动障碍,本病是和青少年最常见的精神。目前国内仅河南中帅科技发展有限公司一家申报,该公司共申报2种剂型:缓释胶囊和片剂,缓释胶囊已获临床批件,片剂也已审评完毕,现处于审批阶段,期待获得临床批件。
3.审批完毕
本周共5个审批完毕的药物,4个化药,1个中药,重点介绍一款海正的1.1类新药:
1.AD-35:本品是一种抗阿尔茨海默症(即治疗老年痴呆症)新药,在美国IND申请已获得批准,目前海正药业载国内1.1类申报本品,原料药已审批完毕,制剂仍旧处于审评阶段,但是从进度来看,已经审评完毕了。本品2013年10月申报,为特殊审批品种,2014年7月发补一次,已批临床。
此外,审批完毕的化药还有济南百诺医药科技开发有限公司3.1类新药盐酸胍法辛缓释片;浙江柏康药业有限公司的6类仿制药头孢呋辛酯分散片;以及湖北多瑞药业有限公司的6类仿制药氯化钠注射液。
4.制证完毕
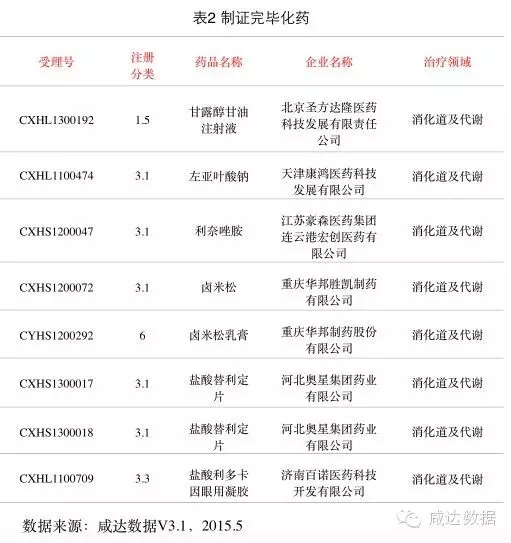
本周制证完毕的药物共10个,其中8个化药,2个中药。北京圣方达隆医药科技发展有限责任公司的1.5类新药甘露醇甘油注射液、天津康鸿医药科技发展有限公司的左亚叶酸钠以及济南百诺医药科技开发有限公司的3.3类新药盐酸利多卡因眼用凝胶均已获批临床。具体信息如下:
关键词:
|