泰博医疗-专业的儿科医疗连锁机构
作者: 发布时间:2015-03-24 转至微博:
|
医药网3月23日讯 3月13日,药品审评中心(CDE)发布了2014年度药品审评报告,详尽地披露了过去一年国内药品的审评审批情况。总体来看,新药申请较平稳,验证性临床和ANDA申请的增长显示仿制药企业的入市决心,而进口再注册的暴增显示出外企对国内市场的积极态度,国内外企业都动起来了!
外企进口再注册品种,裹挟着原研药的余威呼啸而来,看重的是国内巨大的市场需求。国企面对技术及品牌等多方优势的外企,该如何挑战权威?国内产品同样是越发激烈的竞争局面,又将如何突围?这些都成为企业必须思考的问题。
为了提高患者获得最新治疗的可能性及可及性,2014年药审中心批准多个重要治疗领域的药品上市。这为企业的管理者提供了一个思路。这次CDE建议批准9个重点治疗领域的12个品种,涉及抗、抗风湿、疫苗、麻醉镇痛用药、内分泌系统、眼科、消化系统、心血管系统和生殖系统的方方面面。其中品种最多的是肿瘤治疗领域。江苏恒瑞在2013年因甲磺酸伊马替尼片剂和胶囊登上CDE重点领域获批品种后,2014年又因甲磺酸阿帕替尼片再次上榜,显示出强大的研发实力。
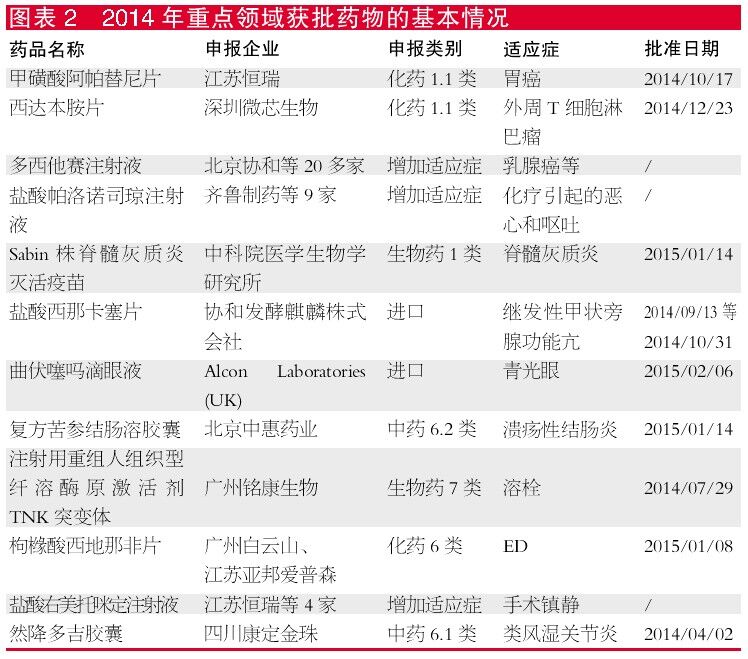
从重点领域建议批准药物的特点来看,除填补国内空白的一类新药外,CDE重点关注的还有能够与国际同步的新适应症,以及更优的疗法和更优的价格等。
鼓励创新、填补空白
代表品种:甲磺酸阿帕替尼、Sabin株脊髓灰质炎灭活疫苗
首先说说一类新药。在靶向治疗癌症的酪氨酸激酶抑制剂大行其道的今天,从2011年浙江贝达的“凯美纳”(盐酸埃克替尼)获批,到2014年江苏恒瑞的“艾坦”(甲磺酸阿帕替尼)批文的获得,标志着我国酪氨酸激酶抑制剂的研发已获得长足发展。浙江贝达年报显示,2013年“凯美纳”的销售额达到4.75亿元,而且增速惊人。这预示着恒瑞的“艾坦”上市后的销售情况可以大胆憧憬。
中科院医学生物学研究所的“Sabin株脊髓灰质炎灭活疫苗”,作为全球首个Sabin株脊髓灰质炎灭活疫苗(单苗),不仅填补了我国在脊髓灰质炎灭活疫苗生产领域的空白,而且对我国乃至全球,特别是发展中国家消灭脊髓灰质炎都会产生积极的影响,是功在当代、利在千秋的大事。
关键词:
|